韩敬东/周永合作利用人工智能鉴定生物年龄、衰老速率和生活习惯的影响
日期:2020-09-08 浏览次数:14317
来源:BioArt
衰老是众多复杂疾病的主要风险因素。同样年龄的个体,其实际的生理年龄差异很大。现有的衰老研究大多基于寿命,而不是衰老本身。衰老与寿命并不能等同,比如有俗称的“好死不如赖活着”的长寿。而衰老研究的目的是为了更健康的晚年生活。系统定量的衰老速率模型,又被称为衰老时钟,正是为了来计算生物年龄,然后用生物年龄与实际年龄的差值作为衰老速率来量化个体间衰老程度的差异。实际操作中,由于生理年龄金标准的缺失,往往用实际年龄代替生物年龄来训练时钟模型,据此来定义离群值,并用其他的生理或分子参数作为佐证。现有方法都是基于这样的操作。譬如,使用人外周血单核细胞转录组芯片数据来预测人的年龄,得到的实际年龄与预测年龄之间的误差为7.8岁【1】,而使用人全血全基因组甲基化芯片数据(基于Illumina 27K芯片)得到的误差为4.9岁【2】。利用这些方式都需要血液细胞,测量的侵入性和高费用使得他们不可能应用于大规模筛选或常规体检。这就限制了生理年龄测量在这个人口老龄化时代的推广应用与社会意义。2015年北京大学、中国科学院上海营养与健康研究所(中国科学院-马普学会计算生物学伙伴研究所)韩敬东研究组首次发表了基于三维面部图像预测年龄的方法,受到了世界各地媒体的报道。这项技术当时的误差为6.2岁【3】,它比起其它衰老时钟有着无创廉价的优势,因此可以快速大规模收集数据,建立更精确的人工智能模型。2020年9月7日,韩敬东研究组与上海交通大学附属第一人民医院临床研究院周永研究组合作在Nature Metabolism上发表了题为Three-dimensional facial-image analysis to predict heterogeneity of the human ageing rate and the impact of lifestyle的研究论文。在此前的三维面部图像预测年龄的方法基础上,这项新发表研究在近五千人的三维面部图像上训练深度学习模型,这一非线性年龄预测模型可以达到与实际年龄或目测年龄误差仅为2.79/2.90岁。目测年龄是生物年龄的衡量标准之一,目测年龄预测模型的建立标志着可以直接通过人工智能学习人类鉴定生物年龄的过程,而不是之前这一领域的方法论中间接地用预测年龄与实际年龄的差值来估测生物年龄,从而规避了原先把预测误差当作衰老速率的假设。通过这一模型,研究者发现个体衰老速率的异质性在中年时期达到峰值。通过280个外周血单核细胞的转录组测序样本,研究者发现了与衰老速率最为相关的生物学过程与细胞类型。
该研究综合了转录组数据、三维面部数据与生活方式调查数据三项因素,为研究者通过使用因果推断的方式,找到将三者维系在一起的分子中介提供了一个前所未有的机会。研究发现吸烟与衰老速率呈正相关,其中介分子是SEMA6B、GRN等细胞因子,其他不良的生活习惯如酗酒、食用腌制类食品等也与衰老速率呈正相关。相反的,食用酸奶、咖啡、水果、鸡、豆类等以及按时吃饭都与衰老速率呈负相关关系,其中介分子包括了组蛋白乙酰化酶复合体蛋白ZZZ3的升高、SEMA6B and SMAD1等的降低。
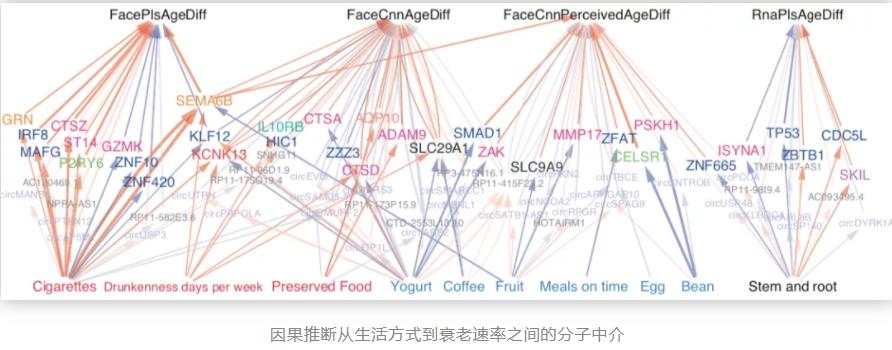
最后,这些可视化结果存储在人类血液基因表达与三维面部图像的关联(human blood gene expression – 3D facial image association, HuB-FI)数据库(https://www.picb.ac.cn/hanlab/hub-fi)中,供其他研究者与公众查询。
据悉,该研究工作主要由韩敬东研究组夏娴博士与陈兴委博士作为共同第一作者合作完成,韩敬东教授与周永教授为通讯作者,并得到了Carlo Vittorio Cannistraci、张康、Brian Kennedy、王嵬教授的帮助。https://doi.org/10.1038/s42255-020-00270-x
1. Peters, M. J., Joehanes, R., Pilling, L. C., Schurmann, C., Conneely, K. N., Powell, J., . . . Johnson, A. D. (2015). The transcriptional landscape of age in human peripheral blood. Nature Communications, 6, 8570. doi:10.1038/ncomms95702. Hannum, G., Guinney, J., Zhao, L., Zhang, L., Hughes, G., Sadda, S., . . . Zhang, K. (2013). Genome-wide Methylation Profiles Reveal Quantitative Views of Human Aging Rates. Molecular Cell, 49(2), 359-367. doi:10.1016/j.molcel.2012.10.0163. Chen, W., Qian, W., Wu, G., Chen, W., Xian, B., Chen, X., . . . Han, J. D. (2015). Three-dimensional human facial morphologies as robust aging markers. Cell Res, 25(5), 574-587. doi:10.1038/cr.2015.36


