

高璞/章新政合作揭示Type I R-M系统的组装、催化和调控机制
日期:2020-06-04 浏览次数:8504
来源:BioArt
对病原DNA的免疫识别,是宿主细胞感知病原感染的重要手段,这种免疫响应广泛存在于从低等原核生物到高等哺乳动物当中(图1)。哺乳动物细胞利用多条天然免疫通路识别病原DNA并介导免疫应答;细菌则主要依赖“R-M系统”及“CRISPR-Cas系统”来去除入侵的噬菌体DNA。
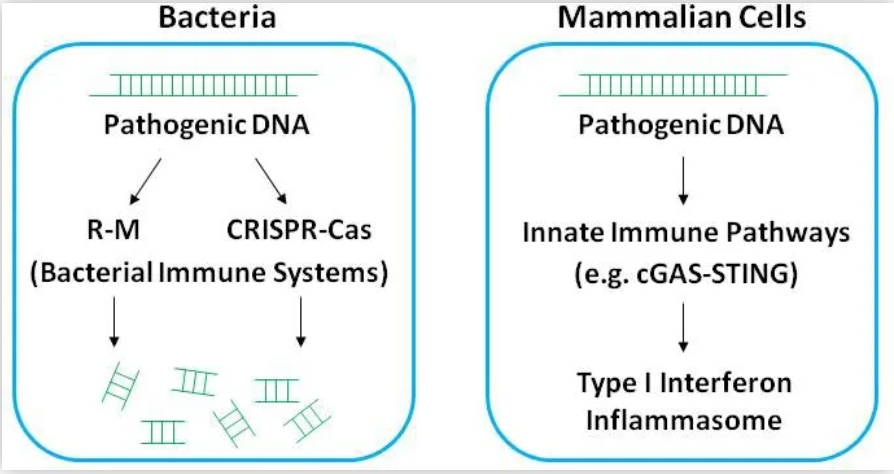
图1:宿主细胞对病原DNA的免疫识别和应答
限制修饰(Restriction-Modification;R-M)系统被称为细菌的天然免疫系统,可对宿主自身DNA进行甲基化修饰,而对未经修饰的外源DNA进行切割。作为最早被鉴定、且最为精巧复杂的R-M系统,Type I R-M系统存在多种亚基组装方式,并拥有DNA methyltransferase、DNA translocase和DNA endonuclease等酶活性。Type I R-M系统的鉴定,促成了其他类型R-M系统的发现并引发分子遗传学革命,围绕限制性酶的研究和应用也获得了1978年的诺贝尔生理医学奖。然而,虽经历了半个多世纪的广泛研究,人们对于Type I R-M 系统如何组装、如何实现多酶活转换、以及如何受到噬菌体蛋白的调控,却仍知之甚少。另外,由于该系统自身存在复杂且频繁的构象变化,获得其多种状态的高分辨率结构信息,一直是领域内极具挑战的问题。
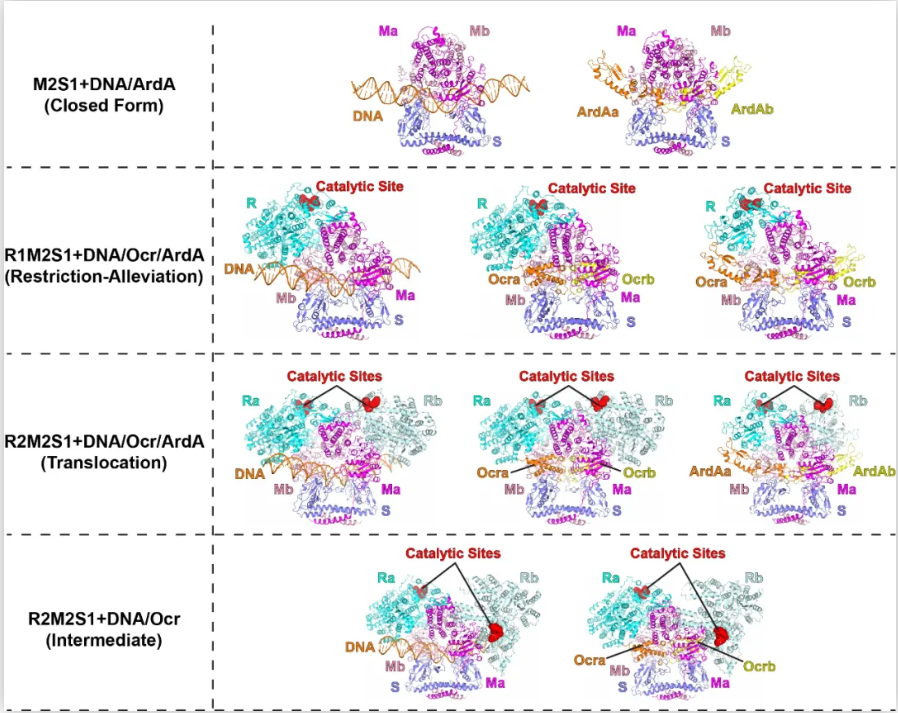
图2:EcoR124I系统与DNA、Ocr及ArdA多种复合物的电镜结构
基于本项研究及前人工作,研究人员提出了Type I R-M全酶的工作模型(图3):(i)未结合靶DNA时,全酶复合物处于一种动态开放的Resting State;(ii)结合靶DNA后,全酶复合物转变为紧凑的Translocation State,并将DNA定位于两个R亚基的Motor-1和Motor-2结构域之间;(iii)通过水解ATP,两个R亚基开始催化DNA translocation,并将DNA从两端拉向Type I R-M复合物,进而形成特殊的DNA loop结构;(iv)当DNA translocation受阻时,Type I R-M全酶转变为Intermediate State,此时仅有一个R亚基具有DNA translocase活性;(v)通过两个R亚基的协同作用,全酶复合物进入Restriction State,两个R亚基的Nuclease结构域和两个M亚基的Catalytic结构域均靠近DNA,发挥DNA切割和甲基化修饰功能;(vi)切割和修饰结束后,全酶复合物与DNA相互分离并返回到初始的Resting State。
