张果/蔡东升/李聚学团队发现肥胖相关脑血管功能障碍的新机制
日期:2020-05-26 浏览次数:8309
来源:BioArt
当前,以肥胖为代表的代谢性疾病群已成为全球性的公共卫生问题。肥胖是多种脑血管疾病,如缺血性脑卒中等疾病的重要危险因素,但其原因还不清楚。脑血管与其他部位血管的组成和结构有所不同。例如,脑血管周围脂肪组织偏少;中枢神经系统里的主要细胞,如神经元、胶质细胞和周细胞等,通过与血管壁中的细胞相互作用,从而调节血管功能。基于这些特点,需要专门开展针对脑血管的研究。2020年5月25日,华中科技大学张果教授、美国爱因斯坦学院蔡东升教授与南京医科大学李聚学教授合作在Nature Neuroscience杂志在线发表了题为Reversal of prolonged obesity-associated cerebrovascular dysfunction by inhibiting microglial Tak1的研究论文。该团队利用实验动物模型,首次发现小胶质细胞内炎症信号通路的过度活化与肥胖伴随的脑血管功能异常相关,阻断该炎症信号通路能够显著改善肥胖小鼠脑血管的病理改变和缺血性脑卒中的预后,揭示了肥胖相关脑血管功能紊乱的机制。
该团队的研究表明,肥胖小鼠的脑干部位出现小胶质细胞(神经系统内一种主要的胶质细胞)增生,以及小胶质细胞中的转化生长因子β活化激酶-1(Tak1)的异常活化,提示发生了炎症反应。另一方面,肥胖小鼠的基底动脉(向大脑供血的主要动脉之一)发生了病理性重构和功能性障碍,表现为血管壁增厚、胶原过度沉积、内皮细胞一氧化氮合酶(eNOS)的活性降低,以及血管内皮依赖的舒张能力受损等。该研究进一步探讨了小胶质细胞中Tak1起源的炎症反应在肥胖相关脑血管功能紊乱中的作用。结果显示,通过药物抑制,或者敲除肥胖小鼠小胶质细胞中的Tak1基因,能够显著缓解其脑血管的病理性结构改变,并改善血管内皮依赖性舒张功能。反之,在正常小鼠的小胶质细胞中持续活化Tak1,会导致其脑血管发生结构异常和功能紊乱。通过分析多种细胞因子和趋化因子,该研究发现,肥胖小鼠脑干小胶质细胞中促炎症细胞因子IL-18的产生显著增加。利用IL-18受体的抗体阻断IL-18信号传导,能够显著改善肥胖小鼠脑血管的病理性变化,增加内皮细胞中eNOS的活性,并增强血管内皮依赖的舒张能力。
最后,该团队研究了小胶质细胞炎症信号通路在肥胖相关疾病——缺血性脑卒中中的作用。具体而言,该研究小组对小胶质细胞特异性敲除Tak1基因的小鼠进行了短暂性大脑中动脉栓塞(MCAO)实验,该实验是在啮齿类动物中研究缺血性脑卒中的常用模型。结果发现,敲除小胶质细胞内Tak1基因的肥胖小鼠,其缺血性脑卒中的预后要明显优于对照组。以上结果说明,小胶质细胞中Tak1和IL-18炎症信号的异常活化在肥胖相关的脑血管功能性障碍中具有重要作用,靶向Tak1和IL-18对于相关疾病的防治可能具有重要意义。
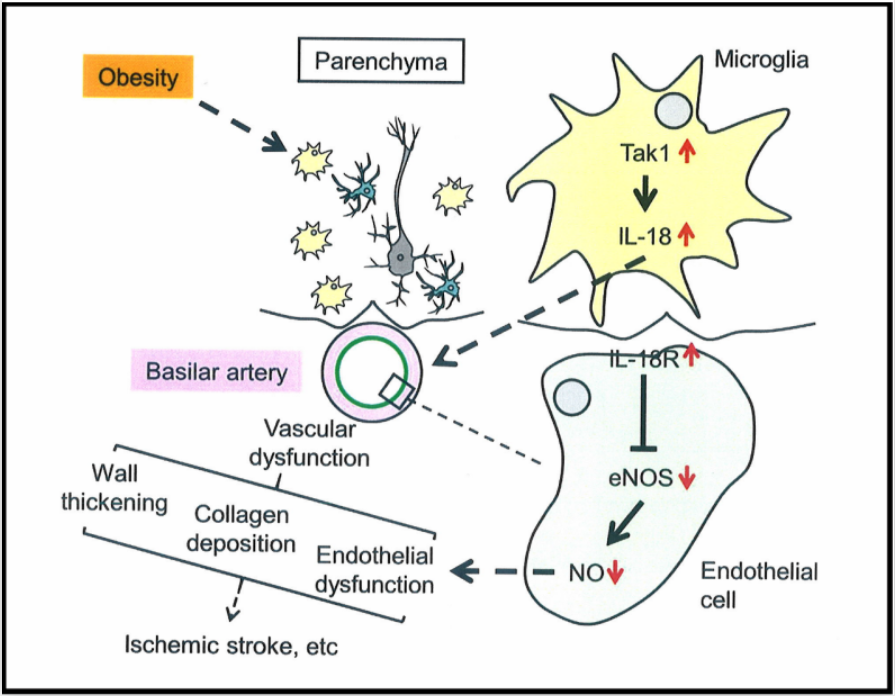 小胶质细胞Tak1-IL-8信号通路在肥胖相关脑血管功能障碍中起重要的作用
小胶质细胞Tak1-IL-8信号通路在肥胖相关脑血管功能障碍中起重要的作用
据悉,张果实验室博士研究生沈青为该论文第一作者。张果教授为该论文通讯作者。美国爱因斯坦学院蔡东升(Dongsheng Cai)教授为该论文共同通讯作者。南京医科大学李聚学教授为该研究做出了重要贡献。张果教授和李聚学教授实验室研究生为该研究提供了大量支持。https://doi.org/10.1038/s41593-020-0642-6


 小胶质细胞Tak1-IL-8信号通路在肥胖相关脑血管功能障碍中起重要的作用
小胶质细胞Tak1-IL-8信号通路在肥胖相关脑血管功能障碍中起重要的作用