饶子和团队解析“药靶-药物”三维结构,揭示一线抗结核药物精确作用机制
日期:2020-04-24 浏览次数:9422
文章来源:BioArt
结核病是当今世界上致死率最高的严重传染性疾病。其人群基数大,影响范围广。目前,治疗结核病的一线药物均为上世纪40-60年代开发,使用已长达半个多世纪。耐药性问题随之产生并且日趋严重,甚至无药医治,给结核病防治带来了前所未有的压力。因此,针对抗结核药物靶点的研究以及新药的研发迫在眉睫。
结核分枝杆菌是引起结核病的病原菌,其细胞壁极为特殊,主要成分包括分枝菌酸(MA)、阿拉伯半乳聚糖(AG)、肽聚糖(PG)和脂阿拉伯聚糖(LAM)等,对结核菌起到天然保护作用。抑制细胞壁成分的合成被认为是合理的抗结核新药研发思路。当前使用的一线抗结核药物异烟肼、乙胺丁醇等均是通过抑制细胞壁合成发挥作用的。研究表明,乙胺丁醇靶向参与AG和LAM合成的阿拉伯糖基转移酶EmbA,EmbB和EmbC。但是自该药物问世以来,其分子机制一直未被解开,这就大大阻碍了乙胺丁醇这一“传统老药”的更新换代和耐药性的解决。饶子和院士团队长期以来致力于针对结核病重要靶点的研究及新药开发。2018年10月25日,团队联合孙飞研究员、王权博士等在Science上发表文章解析了临床药物Q203靶点——呼吸链超级复合体CIII2CIV2SOD2结构;2019年1月24日,与杨海涛教授的合作团队在Cell上发表文章解析了临床药物SQ109靶点——MmpL3的多个“靶点-药物”复合物结构。2020年1月15日,与戈宝学教授团队在Nature发表文章首次发现结核分枝杆菌的重要毒力因子Rv0222分泌蛋白只有在被宿主泛素链接酶ANAPC2催化发生K-11泛素化修饰后,才能招募抑炎蛋白分子,从而阻断宿主抗结核免疫通路,以此揭示了结核分枝杆菌感染治病的新机制。
2020年4月24日,饶子和院士与合作者在Science杂志上以研究长文(Research Article)形式发表了题为Structures of cell wall arabinosyltransferases with the anti-tuberculosis drug ethambutol的研究论文。研究团队再获重大突破,解析了一线药物乙胺丁醇靶点——EmbA-EmbB和EmbC-EmbC两种复合物的三维结构,揭示了乙胺丁醇作用于靶点的精确分子机制。该项成果的取得历经6年漫长的时光,研究团队不畏艰难,相继克服了蛋白样品不表达,晶体衍射分辨率差,相位解析困难,底物难以合成、活性检测体系缺失等诸多难题,最终利用X射线晶体学技术和冷冻电镜三维重构技术,成功解析了Emb蛋白与底物和药物复合物的结构,破解了困扰研究人员长达半个多世纪的抗结核药物机制难题。
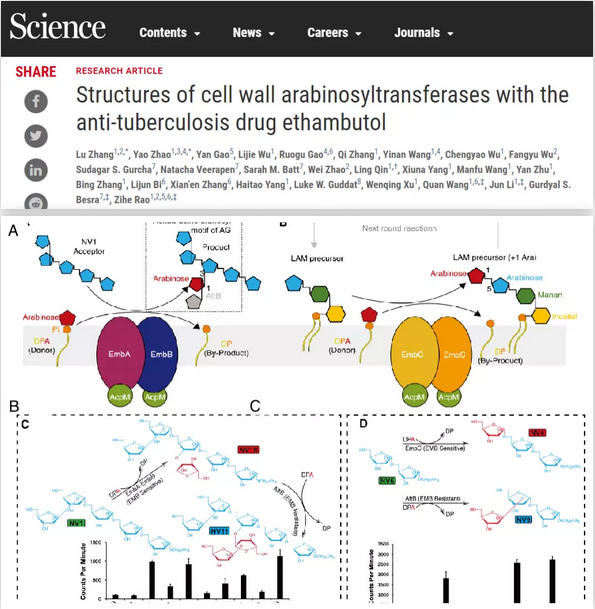
图注:(A)结核分枝杆菌(Mtb)和耻垢分枝杆菌(Msm)EmbA-EmbB-AcpM2和EmbC2-AcpM2与底物(Ara2,DPA)和药物(EMB)复合物结构;(B)以Mtb EmbB为代表展示Emb蛋白结构特征;(C)Emb蛋白拓扑结构示意图
结构研究表明,EmbA和EmbB以异源二体形式,而EmbC则以同源二体形式发挥生理功能。一个令人意外的发现是,参与细胞壁MA合成的AcpM蛋白结合于每个Emb蛋白的胞内侧,分别形成EmbA-EmbB-AcpM2和EmbC2-AcpM2复合体。每个Emb蛋白结构均可划分为一个15次跨膜结构域和两个含有jelly-roll折叠形式的胞外结构域,活性口袋则位于跨膜结构域和胞外结构域之间。研究分析了阿拉伯糖供体(DPA)和二糖(Ara2)在活性位点的精确结合方式。进一步研究发现,乙胺丁醇同样结合于EmbB和EmbC的活性口袋,其结合位点分别占据了催化氨基酸Asp两侧的底物结合位置(D-site 和A0-site),从而同时阻断了阿拉伯糖供体和受体的结合,最终抑制了细胞壁AG和LAM的合成。通过分析乙胺丁醇临床耐药突变位点,团队成员发现大部分位点均位于EmbB和EmbC的药物结合位置附近。相关位点氨基酸的突变可直接或者间接影响到乙胺丁醇的结合。因此,对于解决耐药性问题,需要在新药设计时考虑到避免这些位点的空间影响。以上研究成果将为乙胺丁醇的优化和靶向Emb蛋白的新药开发奠定坚实的结构理论基础。总之,该项工作在国际上首次成功解析了分枝杆菌关键的阿拉伯糖基转移酶复合体EmbA-EmbB和EmbC-EmbC的“药靶-药物”三维结构,揭示了一线抗结核药物乙胺丁醇作用于该靶点的精确分子机制,为解决结核病耐药问题,研发新型抗结核药物奠定了重要基础。
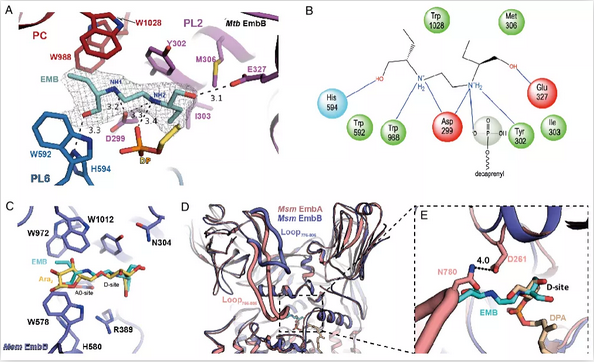
图注:(A,B)乙胺丁醇结合方式;(C,D,E)结构叠合发现乙胺丁醇占据底物阿拉伯糖的结合位点(D-site和A0-site)
据悉,本项工作的完成标志着饶子和团队通过多年努力全面攻克了结核病关键药靶领域已知仅剩的几个战略高地。目前,研究团队正充分利用张江生物医药产业基地的优势,通过全面合作,全力推动抗结核新药的研发,加快基础研究成果的转化。上海科技大学2014级博士生赵耀,南开大学张璐博士为论文共同第一作者。清华大学、南开大学教授兼上海科技大学免疫化学研究所特聘教授饶子和院士、英国伯明翰大学Gurdyal S. Besra教授、上海科技大学免疫化学研究所副研究员李俊、上海科技大学免疫化学研究所课题组长兼生命科学与技术学院助理教授王权为论文共同通讯作者。上海科技大学为该项工作的第一完成单位。晶体衍射数据收集得到上海同步辐射光源帮助,电镜数据收集在上科大生物电镜平台完成。https://science.sciencemag.org/content/early/2020/04/22/science.aba9102/tab-pdf



