徐华强/张岩等课题组揭示5-HT4、5-HT6和5-HT7受体的配体识别和G蛋白选择调控机制
日期:2022-06-17 浏览次数:4469
来源:BioArt
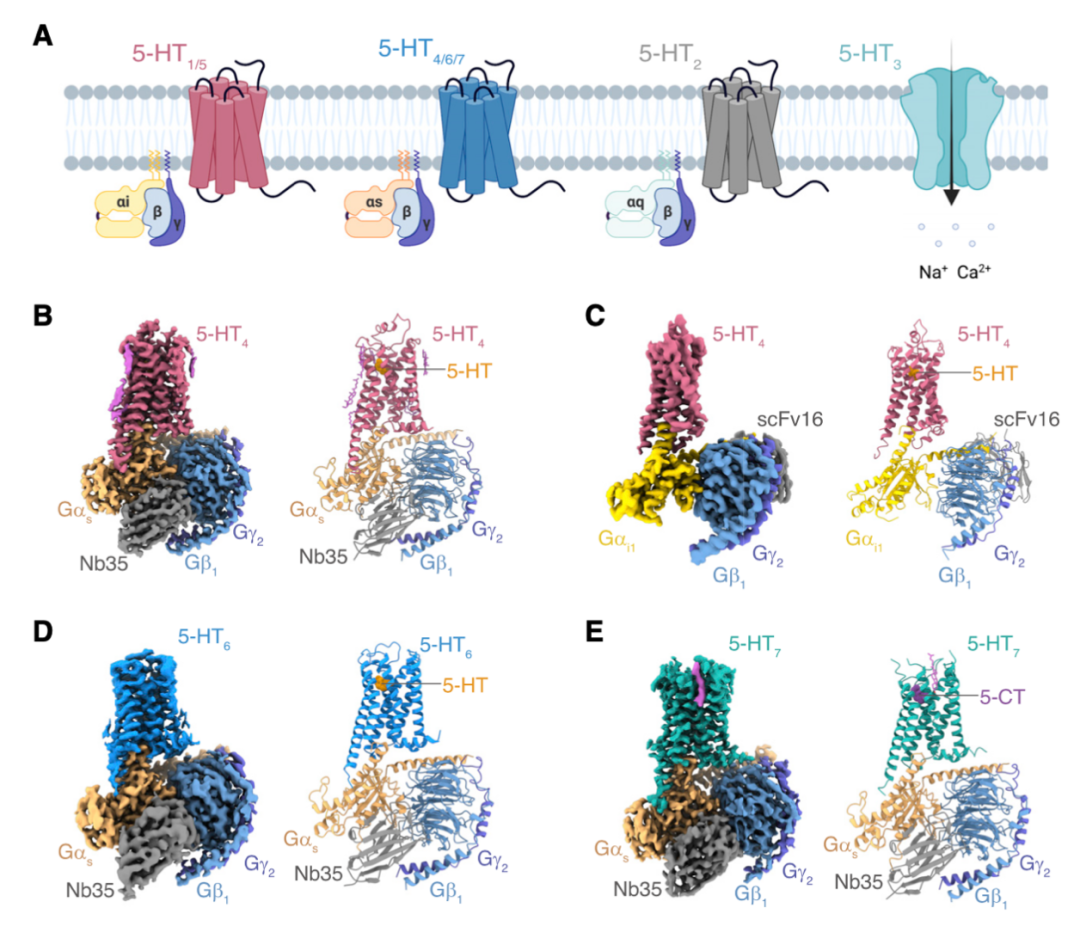
G蛋白偶联受体(GPCRs)是真核生物中最大的一类膜蛋白,在感知胞外信号和介导胞内信息转导中发挥了重要作用,并参与调控多种生理过程,因此与人类疾病密切相关,是最重要的药物靶标蛋白家族。GPCR与第二信使环磷酸腺苷相关的信号通路中,主要通过刺激型G蛋白(Gs)和抑制型G蛋白(Gi)来区分细胞内不同的信号传递方式。了解受体对Gs和Gi信号通路的选择性机制是GPCR和相关信号转导领域长期以来的重要科学问题。5-羟色胺(serotonin, 5-HT)是人体中枢神经系统和周围神经系统的主要神经递质之一,其通过结合5-羟色胺受体(5-HTR)发挥调控食欲、记忆、认知,情绪调节和成瘾等重要的生理过程,这也使5-羟色胺受体成为抑郁症、精神分裂症、偏头痛等疾病的重要治疗靶点。5-羟色胺受体家族是GPCR超家族中最复杂的亚家族之一,其包含12种亚型,不同亚型的受体在人体中发挥不同的生理功能,并且与不同种类的G蛋白偶联。其中5-HT4、5-HT6和5-HT7受体主要偶联下游Gs蛋白,5-HT1和5-HT5受体主要偶联下游Gi蛋白。对于在同一内源性配体5-HT激活后,不同亚型的5-羟色胺受体如何偏好地偶联下游G蛋白来调控细胞应答一直困扰着研究人员。2022年6月16日,中科院上海药物研究所徐华强研究员团队,联合浙江大学张岩教授团队以及丹麦哥本哈根大学的David E. Gloriam教授团队在Molecular Cell杂志上在线发表了文章 GPCRs steer Gi and Gs selectivity via TM5-TM6 switches as revealed by structures of serotonin receptors ,取得了5-羟色胺受体结构和功能领域又一突破性进展,成功解析了5-HT4、5-HT6、5-HT7受体与激活型G蛋白(Gs蛋白)和5-HT4受体与抑制型G蛋白(Gi蛋白)结合的复合物三维结构。他们系统性地揭示了小分子配体5-HT和5-CT识别5-羟色胺受体亚型的结构基础,并阐明了5-羟色胺受体选择性偶联Gs蛋白和Gi蛋白的分子机制。中科院上海药物研究所徐华强研究员联合团队采用单颗粒冷冻电镜技术分别对5-HT激活5-HT4、5-HT6形成的Gs复合物,5-CT激活5-HT7形成的Gs复合物和5-HT激活5-HT4形成的Gi复合物进行了结构重塑,最终解析了4个在配体激活状态下与不同蛋白的复合物结构,其中5-HT-5-HT4-Gs复合物结构的分辨率为3.1 Å,5-HT-5-HT6-Gs复合物结构的分辨率为3.3 Å,5-CT-5-HT7-Gs复合物结构的分辨率为3.2 Å,5-HT-5-HT4-Gi复合物结构的分辨率为3.2 Å(图1)。图1. 5-HT4、5-HT6和5-HT7受体结构该团队将所获的这三种Gs偶联的5-羟色胺受体与Gi偶联的5-羟色胺受体进行了结构比较,且进一步地与另外已发表的19种Gs和Gi偶联的A类GPCRs结构进行比较。他们发现跨膜螺旋TM5和TM6长度作为“macro-switch”来分别确定受体对Gs和Gi的选择性,且这种TM5-TM6 长度的“macro-switch”由A类GPCRs-G蛋白结构共享。此外,TM5和TM6中的特定残基充当“micro-switches”以与Gs或Gi形成特定的相互作用。这些结果展示了A类GPCRs的 Gs和Gi蛋白偶联选择性或混杂的共同机制。为了探究G蛋白偏好5-羟色胺受体的假设,该团队进行了两组实验来检验TM5和TM6的长度是GPCR区分Gs和Gi蛋白的关键因素的假设。第一组实验是将5-HT1A受体的TM6末端螺旋断裂并且TM5螺旋延伸或5-HT4、5-HT7受体的TM5末端螺旋断裂并且TM6螺旋延伸,功能结果表明这种改造影响了5-HT4、5-HT7受体偶联Gs蛋白的能力,然后将5-HT1A受体由原来Gi偶联转变成了Gs偶联,这些结果支持TM5和TM6长度的“macro-switch”是G蛋白选择性的关键。第二组实验是将Gi偶联的5-HT1A的TM5-TM6区域与Gs偶联的5-HT4和5-HT7受体的TM5-TM6区域互换。研究结果表明,嵌合受体5-HT1A (5-HT4_P5.50-P6.50)与野生型5-HT4具有相似的功能,即具有高组成型激活且几乎不受配体调节。同样,5-HT1A (5-HT7_P5.50-P6.50) 显示出与野生型5-HT7相似的功能,在激动剂诱导下进行的cAMP 积累。如果将5-HT4和5-HT7的ICL3替换为5-HT1A,在激动剂诱导下进行的cAMP积累的能力几乎丧失,类似于野生型5-HT1A受体。综上所述,该团队以5-羟色胺家族受体为切入点揭示了A类GPCRs的Gs、Gi蛋白偶联选择性机制,并扩展了5-羟色胺受体的配体识别基础。徐华强团队长期致力于5-羟色胺家族受体的结构与功能研究,并取得了一系列系统性的重要成果。2013年,该团队于在Science上首次报导了激动剂结合的5-HT1B受体的高分辨率晶体结构【1】。2018年,该团队在Cell Discovery发表了首个反向激动剂结合的5-HT1B受体的晶体结构【2】。2021年3月,该团队在Nature上首次报道了5-HT1A、5-HT1D、5-HT1E受体的结构,并揭示了磷脂PI4P(PtdIns4P)和胆固醇调节受体功能的机制和受体的本底激活机制【3】。2021年7月,该团队在Cell Research上首次报道了5-HT1F受体的结构,并揭示了偏头痛药物拉米替坦对该受体的选择性结合机制【4】。2022年5月,该团队在Cell Discovery上首次报道了5-HT5A受体的结构【5】。在前期研究基础上,该成果不仅揭示了A类GPCR选择性偶联G蛋白的分子机制,还填补了5-HT家族受体结构解析的最后空白。该成果首次报道5-HT4、5-HT6、5-HT7受体结构,使所有12种5-HT受体亚型的结构均得到了解析。这些在5-羟色胺受体上系统性的研究极大地丰富我们对5-羟色胺系统的结构与功能认识,并为开发治疗抑郁症、精神分裂症、偏头痛等疾病的药物提供了重要基础。本课题由徐华强研究员领衔,联合浙江大学张岩教授和丹麦哥本哈根大学的David E. Gloriam教授团队等,精诚合作,全力攻关,并在中国科学院上海药物研究所蒋轶研究员和余学奎研究员的协助下完成。上海药物研究所黄思婕博士和徐沛雨博士、浙江大学基础医学院研究助理沈丹丹和丹麦哥本哈根大学的Icaro A. Simon为本文共同第一作者。
原文链接:https://doi.org/10.1016/j.molcel.2022.05.031
参考文献:
1 Wang, C. et al. Structural basis for molecular recognition at serotonin receptors. Science 340, 610-614 (2013).2 Yin, W. et al. Crystal structure of the human 5-HT1B serotonin receptor bound to an inverse agonist. Cell discovery 4, 1-13 (2018).3 Xu, P. et al. Structural insights into the lipid and ligand regulation of serotonin receptors. Nature 592, 469-473 (2021).4 Huang, S. et al. Structural basis for recognition of anti-migraine drug lasmiditan by the serotonin receptor 5-HT1F–G protein complex. Cell Research 31, 1036-1038 (2021).5 Tan, Y. et al. Structural insights into the ligand binding and Gi coupling of serotonin receptor 5-HT5A. Cell discovery 8, 1-9 (2022).