

范祖森/田勇/朱平平发现肠神经细胞是干细胞自我更新和结直肠肿瘤发生所必需的
日期:2022-05-12 浏览次数:4217
来源:iNature
结直肠癌干细胞 (CSC) 有助于结直肠肿瘤的发生和转移。结直肠癌干细胞位于专门的生态位内,具有自我更新和分化能力。然而,CSC 的生态位调控仍不清楚。
2022年5月11日,中国科学院生物物理所范祖森,田勇及朱平平共同通讯在Neuron在线发表题为“5-hydroxytryptamine produced by enteric serotonergic neurons initiates colorectal cancer stem cell self-renewal and tumorigenesis”的研究论文,该研究表明肠神经细胞是 CSC 自我更新和结直肠肿瘤发生所必需的。肠 5-羟色胺能神经元产生 5-羟色胺 (5-HT) 作为 CSC 自我更新的调节剂。5-HT 受体 HTR1B / 1D / 1F 在结直肠 CSC 中高度表达,并与 5-HT 结合以启动 Wnt / β-catenin 信号传导。
从机制上讲,富含结直肠癌 (CRC) 的微生物群异戊酸代谢物抑制 NuRD 复合物富集到 Tph2 启动子上以启动 Tph2 表达,从而导致 5-HT 产生。 5-HT 信号与 CRC 严重程度相关。阻断小鼠体内的 5-HT 信号不仅可以抑制结直肠 CSC 的自我更新,而且还显示出对 CRC 肿瘤的治疗效果。总之,该研究结果揭示了肠神经元和肿瘤细胞之间的串扰,作为 CSC 调节的附加层。
CSCs 受多种信号通路的调控,包括 Wnt/β-catenin、Notch 和 Hedgehog 信号通路。这些通路也在正常成体干细胞中被激活,并且这些通路在正常干细胞中的异常过度激活可能会诱导不受控制的细胞增殖和异常分化,从而以组织特异性方式导致肿瘤发生。因此,这些通路需要受到各种细胞内因子的精确调控,包括长链非编码RNA(lncRNA)、环状RNA(circRNA)、转录因子、染色质重塑因子等。之前鉴定了 lncGATA6、cis-HOX10 和 circREEP3,它们在结直肠 CSC 中高度表达并驱动肿瘤发生。最近,一些利基因子被报道为干性调节剂。然而,肠道神经细胞(肠道中最丰富的细胞之一)是否以及如何调节结直肠 CSC 的自我更新仍然难以捉摸。
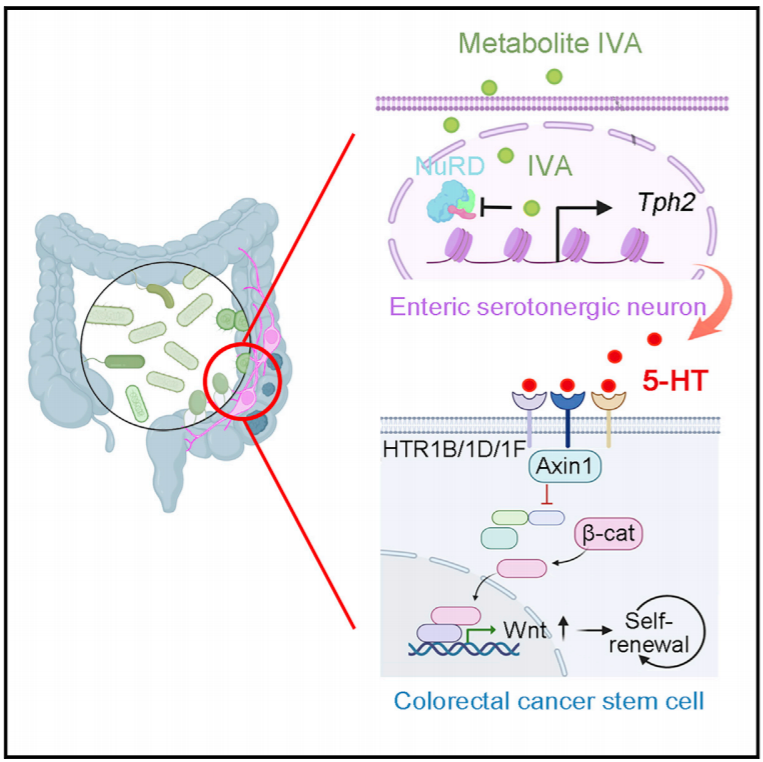
文章模式图(图源自Neuron )
参考消息:
https://www.cell.com/neuron/fulltext/S0896-6273(22)00369-5